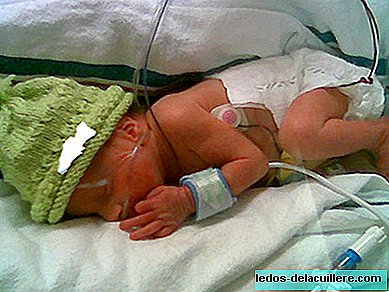
Berikutan kematian 11 bayi di Belanda, selepas menyertai ibu mereka dalam percubaan klinikal dengan Viagra, kami berminat untuk mengetahui apakah peraturan Eropah mengenai kajian-kajian ini pada wanita hamil. Dan lebih khusus, peraturan Sepanyol.
Kerana ... apakah manfaat yang boleh diperoleh dengan mencuba ubat baru benar-benar layak mendapat risiko? Dalam kes tertentu di Holland, nampaknya tidak. Viagra diberikan kepada ibu-ibu masa depan untuk menyelesaikan masalah pertumbuhan janin dan hasilnya adalah bahawa ia memberi kesan kepada paru-paru bayi.
Proses yang perlu dilakukan untuk menjalankan kajian klinikal adalah telus dan terkawal. Tetapi untuk kemudahan menggunakan atau tidak pada ibu mengandung dan menyusui Ini adalah praktikal keputusan penyelidik, seperti yang dapat dilihat dalam undang-undang yang sedia ada. Tetapi mari kita pergi dalam bahagian. Pertama, mari kita lihat apa tujuan kajian ini.
Apakah percubaan klinikal?
Ini adalah penyelidikan perubatan yang dijalankan pada orang, yang menyertai secara sukarela dalam kajian ini, untuk mencari cara yang lebih baik untuk merawat, mencegah, mendiagnosis dan memahami penyakit yang menjejaskan manusia.
Mereka boleh digunakan untuk menguji keberkesanan ubat-ubatan baru atau untuk membandingkan rawatan sedia ada dan menentukan mana yang lebih baik.
Sebelum menjalankan ujian manusia, kajian keselamatan dan keberkesanan lain dijalankan di makmal dan, jika terapi yang sesuai dipertimbangkan, penyelidikan berterusan dan ujian klinikal dijalankan dengan orang.
Setiap ujian klinikal yang dijalankan mesti ditadbir oleh suatu protokol yang menerangkan rancangan yang akan mengikuti kajian tersebut, iaitu, bagaimana ia akan dilakukan dan mengapa perlu untuk membangunkannya, kriteria inklusi dan pengecualian bagi peserta, antara lain Anda juga perlu menunjukkan fasa kajian yang anda ada (satu hingga empat).
Di sini di Sepanyol
Di negara kita, penyelidikan semacam ini ditadbir oleh Dekri Diraja 1090/2015, 4 Disember, yang mengawal selia ujian klinikal dengan ubat-ubatan, Jawatankuasa Etika Penyelidikan Dadah dan Pengajian Klinikal Pendaftaran Sepanyol .
Menurut Kementerian Kesihatan, Keputusan Kerajaan ini berfungsi untuk mempermudah prosedur yang diperlukan untuk menjalankan uji klinik dan dengan demikian menarik penyelidikan dengan ubat-ubatan di Spanyol, menyamai peraturan Eropah. Di samping itu, ia juga memberi peranan yang lebih aktif untuk pesakit dalam membuat keputusan yang memberi kesan kepada mereka sejak, buat kali pertama, mereka wajib dimasukkan ke dalam Jawatankuasa Etika, yang penting untuk meluluskan atau bukan percubaan klinikal.
Di Sepanyol pendaftaran atau pengkomersilan ubat baru tidak dibenarkan tanpa kajian klinikal sebelum ini yang menunjukkan keberkesanan dan keselamatannya untuk kegunaannya. Oleh itu, penyelidikan klinikal adalah perlu dan dalam beberapa kes wajib.
Dan apa undang-undang tentang wanita hamil? Ia hanya merujuk khusus kepada percubaan dalam wanita hamil dalam artikelnya 8, di mana ia mengatakan bahawa:
"Satu percubaan klinikal hanya boleh dijalankan dengan wanita hamil atau menyusu jika, sebagai tambahan kepada syarat-syarat yang ditetapkan dalam pasal 3 hingga 6 dari keputusan diraja ini, semua syarat yang disenaraikan dalam pasal 33 Peraturan (EU) n. No. 536/2014 Parlimen Eropah dan Majlis, 16 April 2014. "
Kami kemudian mengkaji artikel 3 dan 6 Dekri Diraja ini dan mengesahkan bahawa mereka mempunyai watak umum untuk semua peserta yang mungkin dalam sebarang kajian. Khususnya mereka adalah keperluan etika, perlindungan data dan persetujuan yang dimaklumkan. Iaitu, ia menetapkan bahawa untuk menjalankan ujian, peserta mesti memberi persetujuan mereka secara nyata dan data yang dikumpul hanya boleh didedahkan jika mereka menerimanya, dan dari kesamaannya. Mereka sama dengan orang-orang Kesatuan Eropah.
Antaranya, dua mata yang berkaitan dengan peristiwa tragis di Belanda:
"Manfaat yang dijangkakan untuk subjek perbicaraan atau untuk kesihatan awam membenarkan risiko dan kesulitan yang dapat dijangka, dan pematuhan terhadap keadaan ini sentiasa dipantau. Namun, hak, keamanan, martabat dan kesejahteraan subjek yang diguna pakai atas apa-apa kepentingan lain. "
"Akses kepada amalan klinikal yang biasa untuk patologi mereka akan dikomunikasikan kepada orang yang mengambil bahagian dalam perbicaraan, terutamanya dalam kes orang yang mempunyai kelemahan khusus."

Peraturan Kesatuan Eropah
Sejurus selepas itu, kami mencari Peraturan (EU) No. 536/2014 Parlimen Eropah, yang disebut dalam perintah Sepanyol. Dan, khususnya, kita membaca artikel 33, satu-satunya yang merujuk kepada wanita hamil. Terdapat syarat-syarat yang diperlukan untuk menjalankan percubaan klinikal ibu-ibu dan bayi masa depan:
Esei mesti menghasilkan faedah langsung bagi wanita hamil atau bayi terjejas, atau embrio, janin atau anak selepas kelahiran, yang melebihi risiko dan beban yang terlibat.
Bahawa kajian ini tidak dapat dijalankan, dengan keberkesanan yang sama, pada wanita yang tidak hamil atau menyusu.
Bahawa penyelidikan menyumbang kepada pencapaian hasil yang mampu memberi manfaat kepada wanita hamil, bayi, embrio lain, janin atau anak-anak, atau dalam kes-kes yang berkaitan dengan pembiakan.
Ini melibatkan risiko yang minima untuk wanita hamil atau semasa penyusuan, embrio, janin atau anak anda selepas lahir.
Apabila kajian dilakukan terhadap wanita yang menyusu, Langkah berjaga-jaga khas perlu diambil untuk mengelakkan merosakkan kesihatan bayi.
Bahawa tidak ada insentif ekonomi, kecuali pampasan untuk perbelanjaan dan kehilangan pendapatan secara langsung berkaitan dengan penyertaan dalam percubaan klinikal.
Bagaimana jika ada masalah?
Undang-undang Sepanyol (dan juga Eropah) menentukannya sukarelawan mesti menerima pampasan sekiranya mereka mengalami kerosakan akibat percubaan klinikal.
Khususnya, Dekri Diraja 1090/2015, 4 Disember, membincangkan bab III, artikel 9 dan 10, untuk menjelaskan ganti rugi ganti rugi. Ia menyatakan bahawa:
Mereka yang bertanggungjawab untuk memastikan bahawa kajian klinikal memenuhi keperluan adalah Jawatankuasa Etika untuk Penyelidikan Dadah (Ceim), terdiri daripada profesional kesihatan (doktor, jururawat dan ahli farmasi), tetapi juga pakar dalam undang-undang dan bioetika dan sekurang-kurangnya "satu ahli lego, tidak menyedari penyelidikan bioperubatan atau bantuan klinikal, yang akan mewakili kepentingan pesakit ".
Di samping itu, para pengarah kajian bertanggungjawab untuk menyampaikan syak wasangka kesan buruk atau yang tidak dijangka daripada ubat-ubatan yang dikaji ke Agensi Sepanyol untuk Perubatan dan Produk Kesihatan (AEMPS), serta untuk menerbitkan hasilnya, sama ada positif atau negatif.
Di Sepanyol, Undang-undang mengenai jaminan dan penggunaan rasional ubat-ubatan dan produk kesihatan memerlukan pengambilan a insurans liabiliti, atau perlembagaan jaminan kewangan lain, untuk mewujudkan percubaan klinikal, dengan tujuan menjamin liputan ganti rugi yang boleh berlaku di kalangan orang yang mengambil bahagian dalam perbicaraan tersebut.
Langkah-langkah ini hanya mematuhi Peraturan (EU) No. 536/2014 Parlimen Eropah mengenai percubaan klinikal (sudah dirujuk sebelumnya), yang pada titik 62 menyatakan bahawa:
"Negara-negara Anggota mesti memastikan adanya mekanisme pampasan untuk ganti rugi yang mungkin mengalami subjek uji akibat penyertaan mereka dalam percubaan klinikal yang dilakukan di negara mereka".
Persatuan Farmakologi Klinikal Sepanyol menerangkan bagaimana insurans percubaan klinikal dengan ubat-ubatan terdiri daripada.
Sebab-sebab etika yang membenarkan kewujudan insurans untuk menampung kerosakan yang dialami oleh pesakit kerana penyertaan mereka dalam penyiasatan klinikal sangat jelas:
Sekiranya seseorang mengalami kerosakan yang dikaitkan dengan penyertaan mereka dalam siasatan dan mereka tidak akan mengalami jika mereka tidak berada di sana, ia dianggap adil, kerana sumbangan mereka kepada pengetahuan yang dihasilkan oleh siasatan (yang harus dianggap sebagai kebaikan awam ), adalah menghadiri anda secara perubatan secara percuma dan mengimbangi anda secara kewangan untuk kemerosotan kesihatan anda.
Promoter percubaan bertanggungjawab untuk pembelian insurans yang merangkumi ganti rugi., pada masa yang sama dengan tanggungjawab yang boleh ditanggung oleh penganjur, penyiasat utama dan kolaboratorinya.
Ia dianggap sebagai kesalahan yang serius untuk melanggar kewajipan untuk menandatangani jaminan insurans, jaminan atau jaminan kewangan yang setaraf.
Semua perbelanjaan yang diperoleh daripada kemerosotan dalam keadaan kesihatan atau fizikal orang yang menjalani percubaan klinikal akan tertakluk kepada pampasan, serta ganti rugi ekonomi yang diperoleh secara langsung dari kerosakan tersebut, dengan syarat bahawa ini tidak wujud dalam patologi yang di bawah kajian atau evolusi penyakitnya akibat dari tidak berkesan rawatan.
Sebagai jaminan tambahan untuk para peserta, dianggap sebagai kerosakan yang menjejaskan kesihatan anda semasa merealisasikannya dan dalam tempoh satu tahun dikira sejak selesai, mereka telah berlaku akibat perbicaraan.
Dekri Diraja 1090/2015 menetapkan bahawa jumlah minimum yang dijamin sebagai liabiliti ialah € 250,000 bagi setiap orang menjalani percubaan klinikal.
Ia juga membolehkan untuk mengambil modal maksimum yang diinsuranskan setiap percubaan klinikal dan anuiti sebanyak 2,500,000 euro. Maksudnya, jika jumlah semua tuntutan ganti rugi yang diiktiraf kepada semua yang terlibat dalam percubaan yang sama dalam setahun melebihi 2,500,000 euro, syarikat insurans tidak akan bertanggungjawab untuk membayar melebihi jumlah itu, menguraikan jumlah had di kalangan semua yang terjejas
Undang-undang Sepanyol dan Eropah menentukan bahawa sukarelawan mesti menerima pampasan sekiranya mereka mengalami kerosakan akibat percubaan klinikal.Dalam Bayi dan Lebih Pakatan Negeri terhadap Keganasan Gender: kita merumuskan langkah-langkah utama yang memihak kepada wanita dan anak-anak mereka, 11 jawatan untuk menyusu dan mencapai penyusuan susu ibu yang berjaya, apa yang kamu miliki?